
-
خانهخانه
-
مقالاتمقالات
-
فروشگاهفروشگاه
-
طراحی سایتطراحی سایت
-
درباره مادرباره ما
-
حمایت از ماحمایت از ما
-
ارتباط با ماارتباط با ما

اگر این مقاله را دوست دارید، لطفا آن را با دوستان خود به اشتراک بگذارید.
این بررسی نگاه کوچک اجمالی به این می دهد که چگونه فلزات نقش مهمی در زندگی ما دارند. عدم وجود آنها ممکن است باعث بروز بیماری در انسان شود و آنزیم برای عملکرد بدن خود به آنها نیاز دارند. همچنین برای طراحی داروهایی برای درمان بیماری مانند سرطان، آرتریت و استفاده از سوء استفاده از آنها استفاده می شود.
کلمات کلیدی : فلزات، کمپلکس های فلزی، داروهای حاوی فلز، آنزیم های حاوی فلز
یون های فلزی برای سالم نگه داشتن بدن انسان مورد نیاز هستند زیرا دارای عملکرد حیاتی بیولوژیکی در انسان به حضور آنها می باشد و یا ممکن است آنها را تحت تاثیر قرار دهد. با این حال، چند یون فلزی، ویژه یون های به اصطلاحات سنگین، مانند جیوه و سرب، به دلیل فلز سمی خود می تواند خطرناک باشد. یون های فلزی نیز در صورت وجود بیش از حد می توانند سمی باشند، اما وجود آنها برای بقای بسیار مهم است.
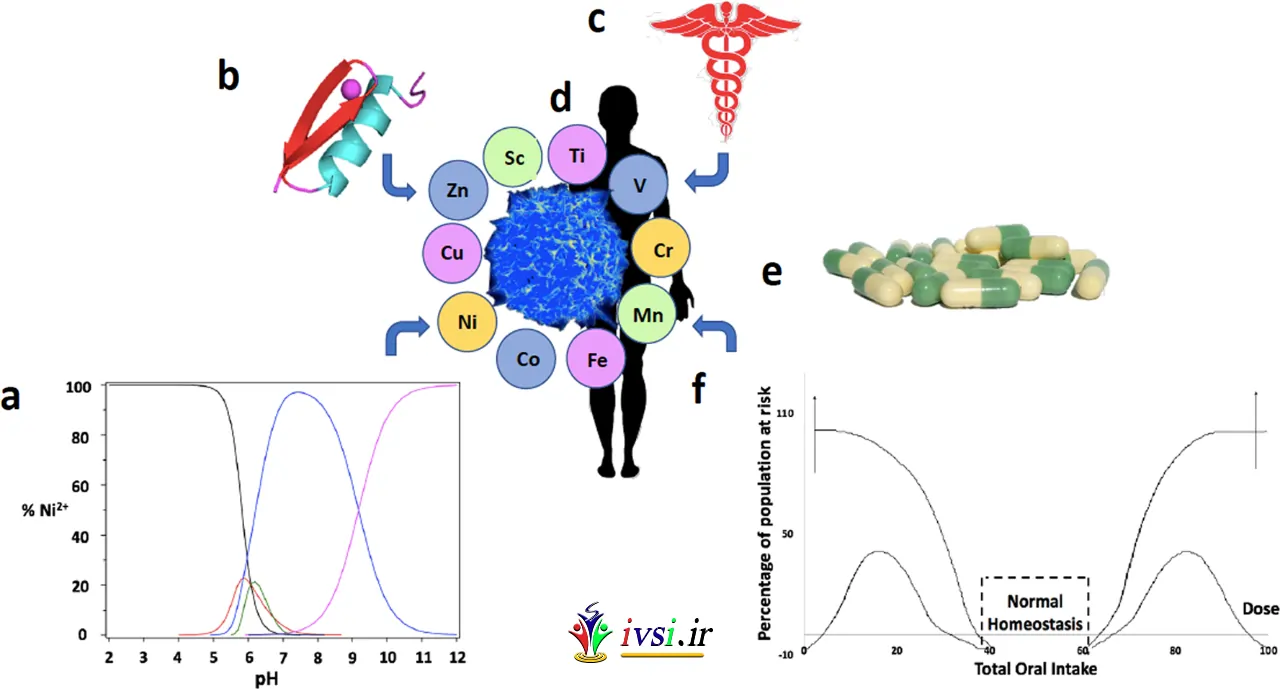
از جمله فلزات در حال حاضر برای عملکردهای بیولوژیکی طبیعی در انسان که مورد نیاز من قرار گرفته اند عبارتند از: سدیم (Na)، پتاسیم (K)، و کلسیم (Ca) که متعلق به گروه اصلی عناصر هستند و وانادیم (V) ). کروم (Cr)، منگنز (Mn)، آهن (Fe)، کبالت (Co)، نیکل (Ni)، مس (مس)، روی (Zn)، مولیبدن (Mo) و کادمیوم (Cd) که متعلق به انتقال هستند. گروه فلزی عناصر جدول تناوبیدر میان این فلزات، قابل توجه ترین فلزاتی است که معمولاً به شکل یون وجود دارند عبارتند از Fe, Co, Ni, Ca, Cu, Zn و Cr. نتایج و کوشش به کم خونی، مسیله به بیماری های مغزی و قلبی و خونی، منجر به کاهش در رشد و تغییرات پوستی، کلسیم به زوال استخوان می شود و کروم باعث کاهش تحمل گلوکز می شود.
بنابراین، اهمیت مهم شیمی بیوان آلی دارویی به مطالعه در سطح بیماریهای مولکولی ناشی از بیماریهای ناشی از یونهای فلزی مختلف و یافتن راههای آنها مربوط میشود . مهمترین جنبه یون های فلزی استفاده از آنها در کشف دارو است. صنعت دارو تنها به یونهای فلزی متکی نبوده، بلکه بر فلزات دیگر متکی است. دوی مهم سیس پلاتین (۱) و اورانوفین (۲) به ترتیب برای درمان تومورهای دستگاه تناسلی و گردن به طور مستقیم استفاده می شوند. یون های فلزات همچنین نقش اساسی در انواع آنزیم ها ایفا می کنند و واکنش های کاتالیز شده توسط آنزیم را با اصلاح جریان الکترون در کنترل ها یا آنزیم ها می کنند.⁶ بدون یون فلزی مناسب، یک واکنش بیوشیمیایی که توسط یک متالوآنزیم خاص کاتالیز ممکن است بسیار کند پیش رود. فلزات می توانند برای اتصال و جهت دهی بستر با توجه به گروه های عاملی در محل فعال عمل کنند. اکنون در اینجا به طور خلاصه شرحی از داروهای حاوی فلزات و همچنین آنزیم هایی که اساساً به فلزات نیاز دارند می سازند.
 |
بخوانید: با رعایت این نکات، تعطیلاتی سالم خواهید داشت!
بعلاوه بر سیس پلاتین (۱)، وجود دارو دارد که با پلاتین کمپلکس شده است. سیس پلاتین برای درمان سرطان های سلول زایا، تومورهای تروفوبلاستیک حاملگی، سرطان تخمدان اپیتلیال و سرطان سلول های کوچک ریه و همچنین برای تسکین سرطان های مثانه، دهانه رحم، نازوفارنکس، مری و سر و گردن استفاده می شود. ⁷-⁹ با این حال، برخی از سرطان ها به سیس پلاتین مقاوم هستند ، ¹⁰،¹¹ و علاوه بر آن بر این عارضه جانبی مرتبط با آن یافت شد.
در نتیجه، ترکیب دیگری به نام کربوپلاتین (۳) ساخته شد که سمیت کمی داشت اما اثربخشی آن در سرطان نسبت به سیس پلاتین خیلی برتر نبود. در واقع، برای برخی از تومورها، سیس پلاتین همچنان از نظر درمانی بیشتر از کربوپلاتین بود. تلاش بیشتر برای کاهش سمیت و مقاومت دارویی برای تولید داروی جدید اگزالیپلاتین (۴) که در نهایت در اوت ۲۰۰۲ برای سرطان کولورکتال در ترکیب با ۵-فلوئورواوراسیل (۵-FU) مجوز استفاده در ایالات متحده را دریافت کرد. ¹²،¹³ قبلاً سال در اروپا استفاده می شود.
ساتراپلاتین (۵، JM216)، سایر عوامل ضد نئوپلاستیک بر روی پلاتین، برای درمان سرطان پیشرفته پروستات تحت بررسی است، اما هنوز یکی از سازمان های غذا و داروی ایالات متحده تایید کرده است. با این حال، علیرغم بی اثر بودن ترکیبات پلاتین (IV)، ساتراپلاتین به سرعت در بول های قرمز خون انسان می تواند گل شکل زیستی را تغییر دهد. ¹⁴ ساتراپلاتین آنالوگ مستقیم سیس پلاتین است (۱). تمام آنالوگ های ساختاری سیس پلاتین آرایه ای بسیار مشابه از ترکیبات افزایشی را روی DNA هدف تولید می کنند و بنابراین همه آنها پیامدهای بیولوژیکی مشابه را القا می کنند و می توانند از فعالیت های بالینی واقعاً مکمل داروی اصلی باشند، حتی اگر از نظر نظر داشته باشند. ساختاری متفاوت باشند. ¹⁵-¹⁸
  |
دو کمپلکس تیتانیوم که به عنوان عوامل ضد سرطانی عمل می کنند، تیتانوسن (۶، MTK4) و بودوتیتان (۷، INN) هستند. تیتانوسن فعالیت ضد سرطانی را نشان داد و اولین کمپلکس غیر پلاتینی بود که تحت آزمایشات بالینی به عنوان داروی شیمی درمانی قرار گرفت.¹⁹ در میان کمپلکس های غیر پلاتینی، بودوتیتان (INN) از پیشرفته ترین آنهاست. امروز در حال انجام آزمایشات بالینی است. بودوتیتان در چندین تومور قابل پیوند بسیار فعال است و امیدوارکنندههای را در مدل تومور کولورکتال اتوکتون نشان میدهد که برای وضعیت بالینی بسیار پیشبینیکننده است.²⁰
 |
روتنیوم ترکیباتی را با بیشترین امید تولید کرده است، هنوز هیچ آنالوگ مستقیمی به کلینیک نرسیده است. NAMI-A (8) و KP1019 (9) دو عامل ضد سرطانی روتنیم هستند که آزمایشات بالینی شده اند. در حالی که NAMI -A در برابر متاستاز ریه در داخل بدن و سلول های تهاجم در شرایط آزمایشگاهی فعال است، KP1019 ²³-²⁵ برایتومورهای متاستاتیک و تومورهای مقاوم به سیس پلاتین مفید است. این سمیت سلولی قوی در برابر تومورهای اولیه، به ویژه در سرطان کولورکتال نشان می دهد.²⁶
 !–شکل از اینجا شروع می شود–> |
برخی از ترکیبات حاوی بیسموت به دلیل خاصیت ضد اسیدی و قابض در انواع اختلالات گوارشی استفاده می شود. یک ترکیب مهم، بیسموت ساب سالیسیلات (۱۰ ، Pepto -Bismol)، یک داروی ضد اسید است که برای درمان ناراحتیهای موقت معده و دستگاه گوارش، مانند اسهال، سوء هاضمه، سوزش سر دل و حالت استفاده میشود. چند ترکیب دیگر در دست توسعه هستند.
| < –شکل از اینجا شروع می شود–>
|
دو کمپلکس طلای اورانوفین (۱۱) و آئوروتیوگلوکز (۱۲) که به نام تیوگلوکز طلا نیز شناخته می شود، برای درمان آرتریت رومات ساخته شده است. اورانوفین علائم آرتریت از جمله مفاصل دردناک یا حساس و متورم و سفتی صبحگاهی را بهبود می بخشد.²⁹ Aurothioglucose همچنین برای درمان آرتریت رومات ساخته شده و بیش از ۷۰ سال از آن استفاده می شود، ³⁰ اما اخیراً از بازار ایالات متحده به همراه مجتمع های طلای دیگری که برای درمان آرتریت رومات ساخته شده بودند، متوقف شدند و تنها اورانوفین به عنوان تنها بودند. نمک طلا روی آن باقی می ماند. بازار آمریکا
< –شکل از اینجا شروع می شود–>
 |
تعداد زیادی آنزیم حاوی فلزات هستند و این گونه آنزیم ها به عنوان متالوآنزیم می شوند. در تمام متالوآنزیم ها، یون فلزی با یک محل هماهنگی ناپایدار به ارتباط می شود و یون فلز معمولاً در یک پاکت قرار می گیرد که شکل آن را با تخت می کند. شکل محل فعال در همه آنزیم ها بسیار مهم است. در تمام متالوآنزیم ها، یون فلزی واکنش نشان می دهد را کاتالیز می کند که در شیمی آلی به سختی به دست می آید. این متالوآنزیم ها کربنیک انیدراز، آنزیم های وابسته به ویتامین B12، نیتروژناز، سوپراکسید دیسموتاز، تامین کننده های حاوی کلروفیل، هیدروژنازها، ریبوزیم و دئوکسی ریبوزیم و متالوپروتازهای ماکس هستند. علاوه بر این، حدود نیمی از تمام مواد غذایی حاوی یک فلز ³¹ هستند که برای انجام وظایف خود نیاز دارند. ³²
در آنزیم ها، یون های فلزی به طور کلی دارای بار مثبت هستند و به عنوان الکتروفیل عمل می کنند و بنابراین با هر نوکلئوفیل وارد برهمکنش بار-بار می شوند. گروه ها یا اتم هایی که به یون های فلزی متصل می شوند دارای بار منفی یا خنثی هستند و بنابراین چگالی الکترونی را به یون های فلزی اهدا می کنند. اتصال مناسب سوبسترا در محل اتصال آنزیم به شدت توسط محیط الکترواستاتیک در محل فعال کمک میکند و یونهای فلزی در اینجا نقش بیشتری دارند و عملکرد آنزیم را میسازند. یونهای فلزی شکلگیری حالت واکنشی را که باید کاتالیز شود را میسازد و آزاد میکند، به آسانی میشود. در بسیاری از سیستم های آنزیمی، یک یون فلزی با یک مولکول آب برهمکنش می کند.
اگر یک مولکول آب به یون های H + و OH – تجزیه شود، OH–به عنوان یک دوست در واکنش های شیمیایی یا بیوشیمیایی عمل می کند. چنین دوستی با فعال شدن مولکول آب در محل به دست می آید و بنابراین یک واکنش شیمیایی به شیوه ای استریو شیمیایی کنترل شده در محل فعال آنزیم رخ می دهد. در عملکردهای کاتالیزوری خود، متالوآنزیم ها از یکی از معدود آرایش بعدی ممکن است گروه های عاملی در اطراف یون فلز استفاده می کنند تا از ویژگی واکنش بیوشیمیایی مورد نیاز اطمینان حاصل کنند. در ساختارهای کریستالی بسیاری از متالوآنزیمها ، پیکربندی برنامهای شامل یک گروه کربوکسیل است که در آن یک ماده که به یون فلز و اتم دیگر به آب متصل به فلز مرتبط است تا ساختار حلقوی ایجاد کند. ³⁴-³⁷ آنزیم های زیادی مانند همیترین، آلکالین فسفاتاز و سوپراکسید دیسموتازها وجود دارند که دو یون فلزی در محل فعال خود دارند.
در هیدرولیز پیوند آمیدی توسط متالوپروتئینازهایی که حاوی روی به شکل روی ۲+ هستند، روی ۲+ عموماً به سه گروه دهنده از آنزیم و یک مولکول آب که هندسه چهار وجهی را به دست میآورد هماهنگ میشود ⁹ هیدرولیز همانطور که در شکل ۱ نشان داده شده است انجام میشود. برای متالوپروتئینازهای ماتریکس (MMPs)، یک کلاس اصلی از متالوپروتئینازهای حاوی روی. گروه های دهنده از آنزیم ممکن است باقیمانده های His (N)، Glu(O)، Asp (O) یا Cys (S) باشند که در آن His رایج ترین است. در مثال برای یک MMP، شکل ۱A نشان می دهد که یک مولکول آب در حالی که به روی ۲+ متصل است، به زنجیره جانبی کربوکسیلات باقیمانده اسید گلوتامیک نیز متصل است. Zn²+یون همچنین با سه باقیمانده هیستیدین، His-228، His-222 و His-218 هماهنگ می شود. پیوند مولکول آب به اسید گلوتامیک، مولکول آب را برای حمله هسته دوست به پیوند آمید قیچی فعال می کند که منجر به انتقال پروتون (H + ) به نیتروژن آمید و اکسیژن کربوکسیلات به Zn²+ به صورت چهار وجهی می شود ( شکل ۱B). ). به طور همزمان، انتقال یک پروتون از اسید گلوتامیک به نیتروژن آمیدی نیز رخ می دهد و به دنبال آن فروپاشی واسطه چهار وجهی با تولید یک پل نمکی بین اسید گلوتامیک و آمین آزاد بستر شکافته شده رخ می دهد ( شکل ۱C ). از طریق کاتالیز اسیدی به محصولات فرو می ریزد.
شکل ۲ نشان می دهد که چگونه یک توانایی می تواند با آنزیم های دارای روی مرتبط شود. این یک مطالعه اشعه ایکس را نشان می دهد که چگونه یک توانایی پپتید N-کربوکسیالکیل را با یک MMP، استروملیزین (MMP-3) مرتبط می کند. ³⁸ شکل نشان می دهد که چگونه، علاوه بر آن برای اتصال هیدروژنی. اتم روی اتصال بازدارنده با آنزیم را تثبیت می کند. نقش اتم روی به تفصیل در بررسی گوپتا ارائه شده است. ³⁹ در واقع، از بین تمام فلزات، برای انجام وظایف در سیستم های بیولوژیکی یافت شده است و این به خواص زیر است که توسط Perkin ⁴⁰ اشاره شده است.

شکل ۱۴ اتصال یک بازدارنده MMP با استروملیزین (MMP-3) که نشان می دهد چگونه اتم روی پیوند شرکت می کند. در شکل P1 و P2 به گروههای بازدارنده یا تختی که به محلهای اتصال مربوط میشود که توسط S1 و S2 در آنزیم اشاره شده است، متصل میشوند. نسخه چاپ با اجازه از مرجع ۳۸. حق چاپ ۲۰۰۰ American Chemical Society. |
فلزات نقش بسیار مهمی در زندگی انسان دارند. عدم وجود آنها ممکن است باعث ایجاد بیماری در بدن انسان شود. همچنین از فلزات برای طراحی داروهای مفید درمانی در کنار بیماری مانند سرطان، آرتریت، زخم، و غیره استفاده می شود. فلزات موجود در آنزیم ها به شدت واکنش کاتالیزوری آنها را می سازند.
بخوانید: راهکارهای جذب سلامتی
اگر این مقاله را دوست دارید، لطفا آن را با دوستان خود به اشتراک بگذارید.

![دانلود کتاب: فضای مجازی و سلامت روانی [راهکارهای بهبود روانشناختی در دنیای آنلاین]](https://ivsi.ir/wp-content/uploads/2023/05/virtual-space-and-mental-health-book-300x300.webp)



